「水喔!今天的文章是水喔!」
「又成功水了一篇,好水喔…」
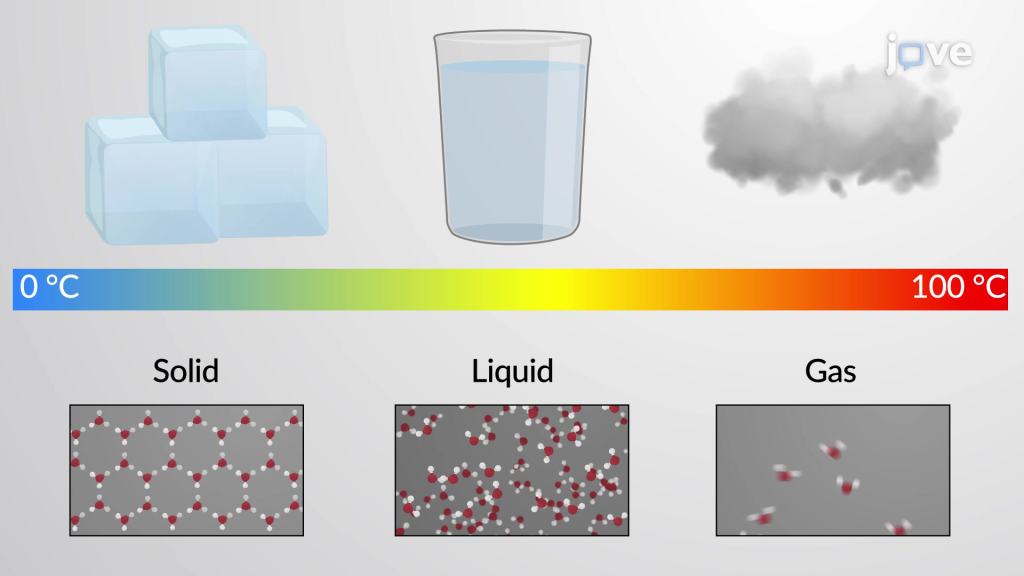
水的三態:固態、液態、氣態(國中範圍,快速跳過)
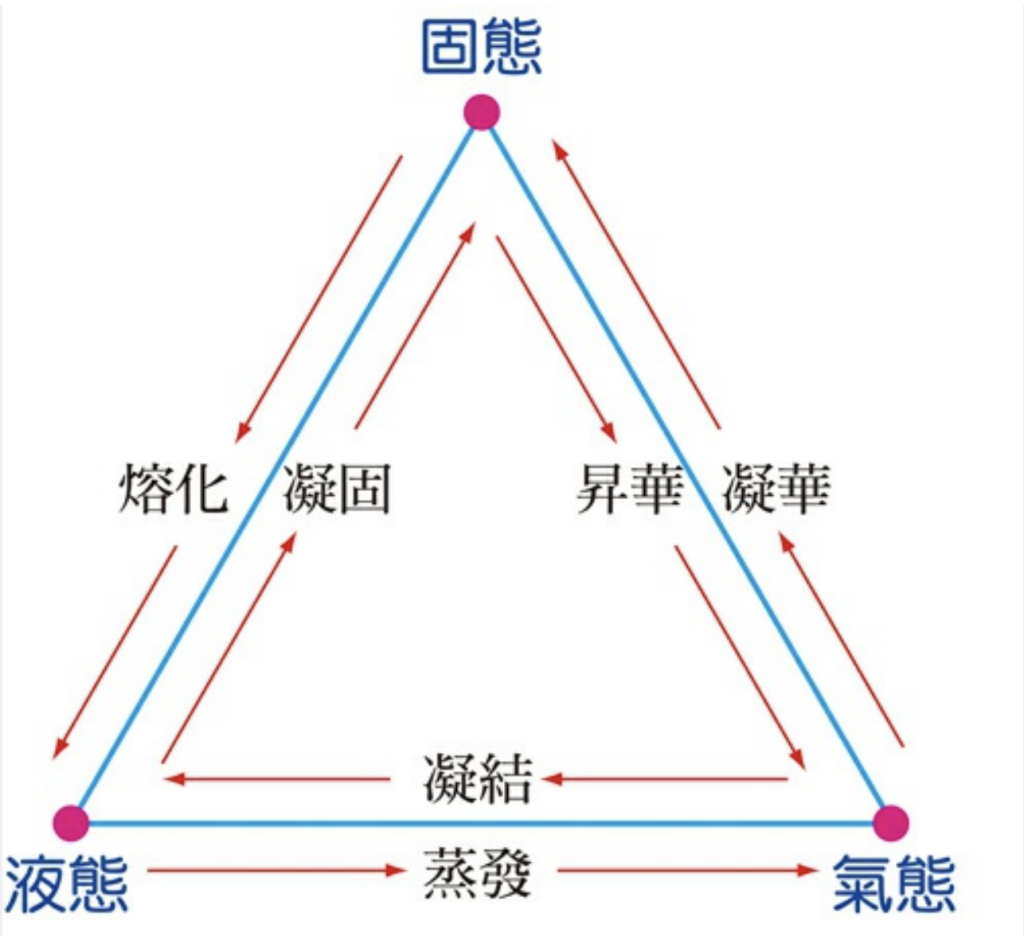
水在 4℃(3.98℃)時密度達最高,熱脹冷脹
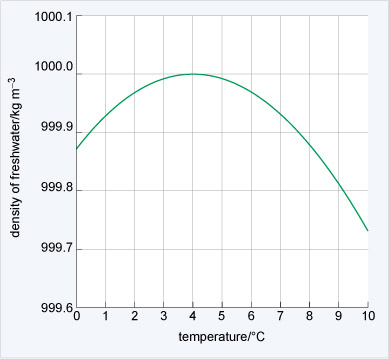
水加熱的完整過程
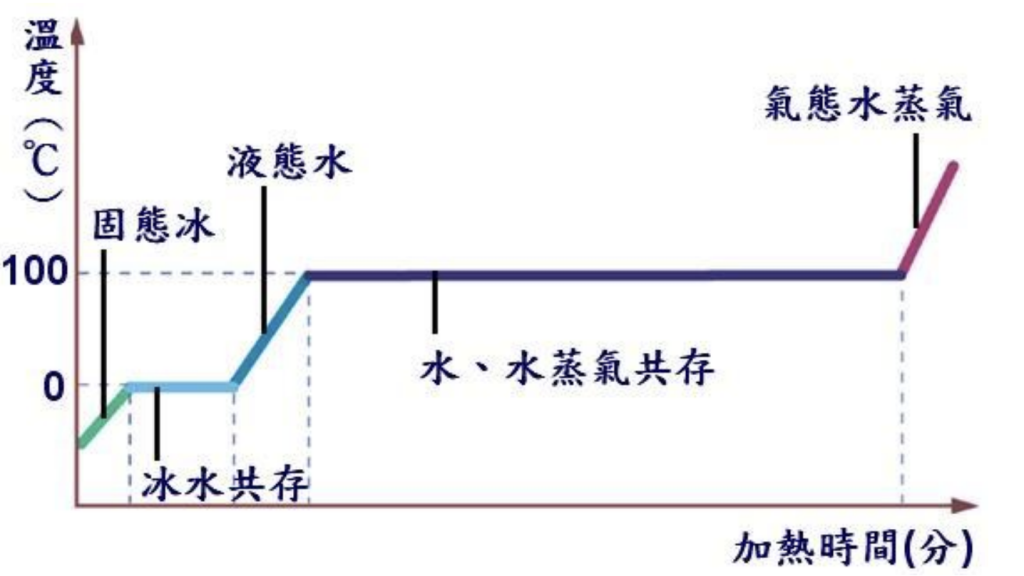
這張圖還藏有另一個含意,加熱時間代表水分子的「位能高低」
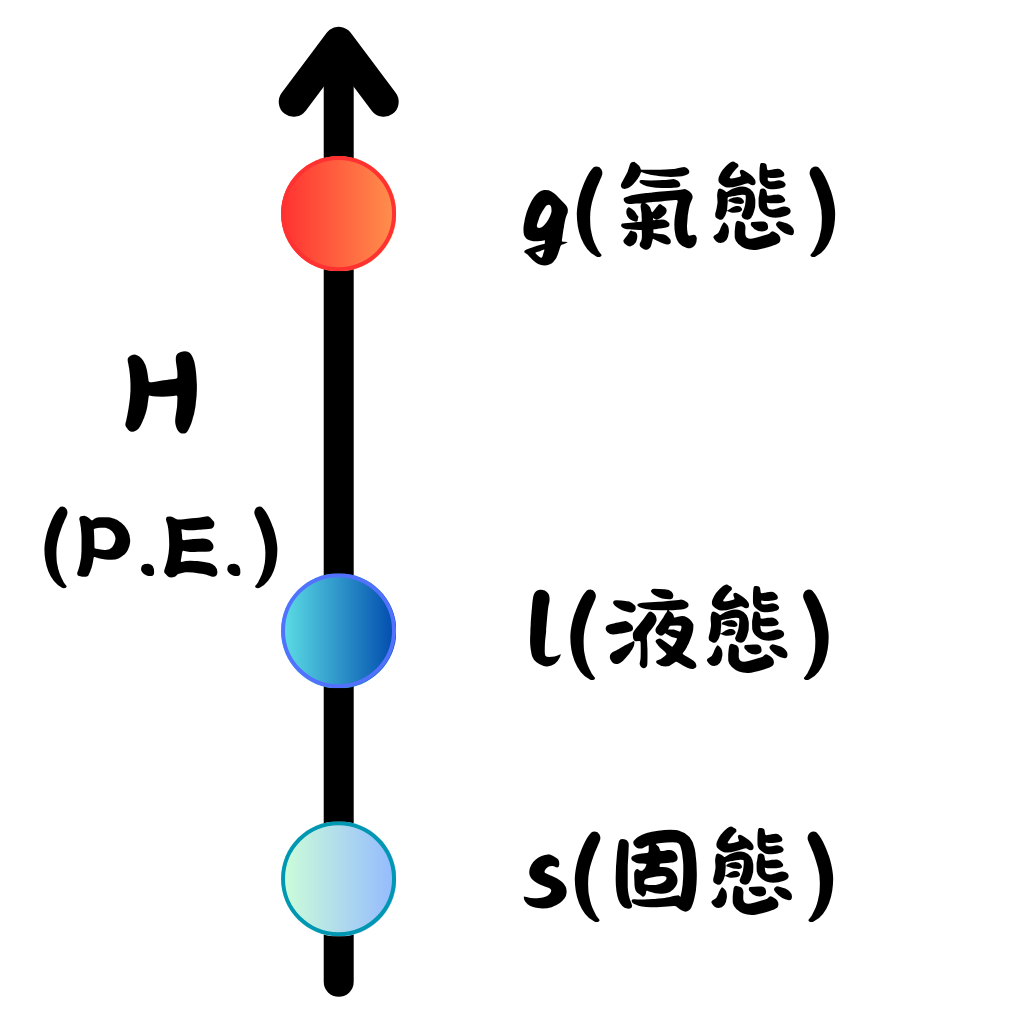
三相位能一定是:固態 < 液態 < 氣態
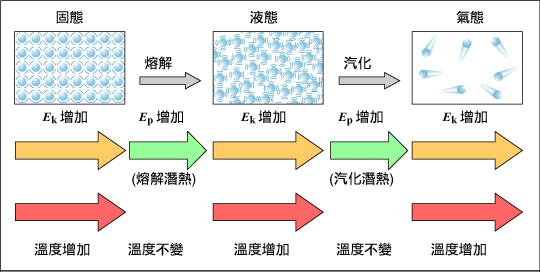
固體若要變成液體、氣體,需要克服分子間的作用力(冰融化、水要變蒸汽,都是靠外界加熱)

分子位能與分子間的距離有關係,通常距離稍遠一些位能會變大
因為能量越高,分子震動的越快、越大力,距離會比原本遠一些
ex: 今天天氣爆幹熱 => 今天分子震動得爆幹快
熱能越大,就能將分子間作用力(分子與分子的吸引力)拆的越遠
就越不穩定、越高位能
原理有一點點…一點點類似物理的「重力位能」公式 E=mgh
(但實際大不相同,不是單純mgh線性關係,而是1/r^6凡得瓦力 之類更複雜的力)
在此處還要考慮超能力(分子間作用力,如氫鍵)
以水為例子,水的密度最高最密緻、冰的密度較小鬆垮
可是按此邏輯
照理說水的位能應該最低,因為兩兩相隔是最緊密、最穩定的狀態
但實際上不是!
因為冰形成了大量氫鍵,抵掉了這位能的影響,所以才是最穩定的狀態
應該說,冰願意犧牲密度與空間效率,來換取整體位能更低的穩定氫鍵結構
冰有最完整、最強的氫鍵 → 勢能最低
液態水氫鍵動態斷裂、再結合 → 勢能居中
水蒸氣幾乎無氫鍵,只剩極弱的分子間作用 → 勢能最高
順帶一提
產生相變化之前必須先「成核(nucleation)」
(雲下雨也是,由人工增雨時,需要搭直升機撒灰塵、塵埃等)
有點像物理上要推動物體時,需先克服「靜摩擦力」
在生活經驗中,水在 0℃ 就結冰了
但實際上,在一個大氣壓 0℃ 以下,不一定 0℃ 就會結冰
低於 0℃ 可以以液態形式存在,但不穩定
稱作「過冷水(supercooled water)」
液體倒出來就結冰,很酷,像在變魔術
(柯南還有一集題材有出現過冷水xd

有「過冷水」,那當然也有「過熱水(superheated water)」
就是超過 100℃ 而不沸騰的,表面看似平靜但充滿危險
產生突然沸騰的「突沸」現象,積累的能量會在瞬間釋放出來
為了避免危險,做實驗加熱時可加入「沸石」(多孔性物質) ex: 陶瓷碎片,避免發生突沸
噢對了
即使水升溫到100度,冰的密度也一定比水還要小
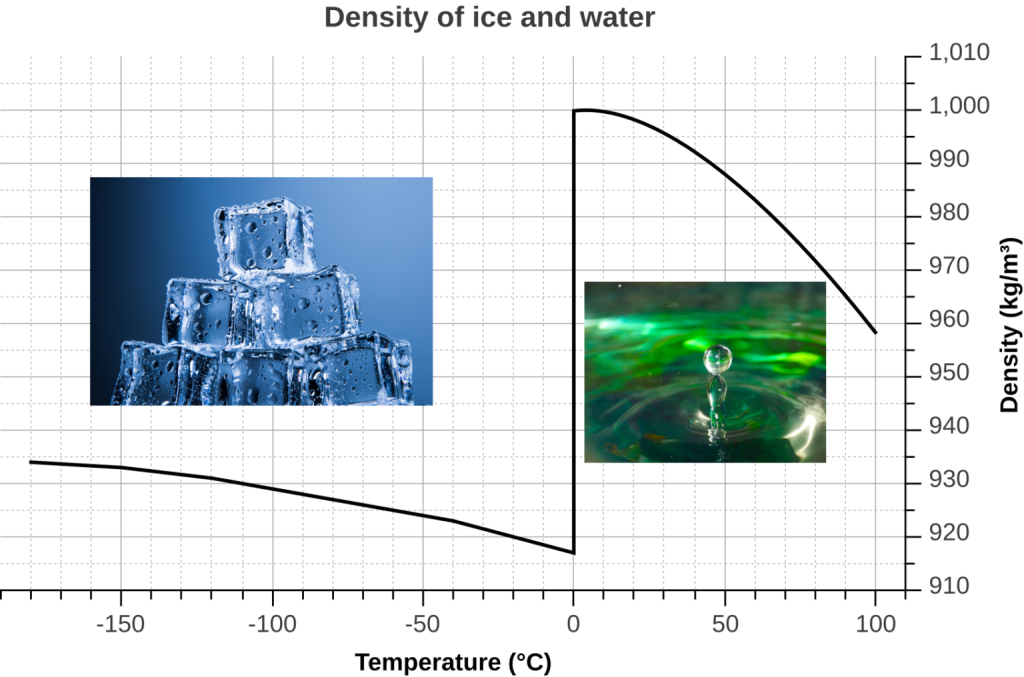
因為結冰後,密度是有個巨大斷層的、跳崖式往下降(結構變化造成密度突變)
「水的最低密度」大約在0.96,而「冰的最高密度」大約在0.93
所以冰塊一定能漂浮在水上
結冰也是從上面開始結冰,因為結冰後會漂浮起來,會跑到上面
但多數物質(酒精、丙酮、水銀、金屬)固化時,則是從下方開始,因為變成固態、結晶後較重,會沉到底部
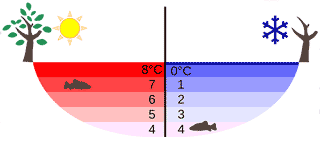
這也是冬天魚可以在冰面下存活的原因,因為最底下有4℃ 的水
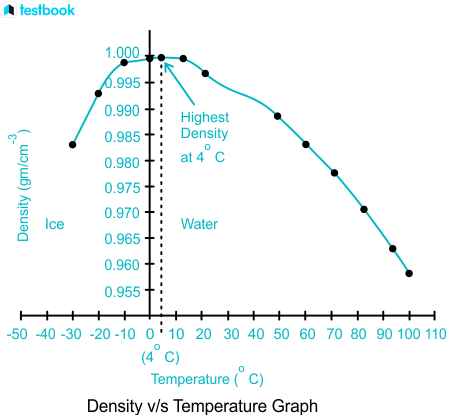
如果有看到這種「非斷層式下跌」的圖,密度線是連續的
那麼低於0度其實是「過冷水」,而不是結冰

發佈留言